Fogos de Artifício – Como funcionam?
Final de ano, nada mais comum que passar a virada do ano vendo o show de fogos de artifício, seja ao vivo ou pela TV. Quem nunca fez isso?
Shows de fogos de artifício são muito bonitos, no entanto, o barulho nas redondezas do espetáculo é gigantesco. E isso, é devido à grande quantidade de pólvora existente em um fogo de artifício.
Composição e Histórico
Um fogo de artifício é composto basicamente por pólvora (mistura de enxofre, carvão e salitre ‘nitrato de potássio’) e por um sal de um elemento determinado (o que irá determinar a cor da luz produzida na explosão).
A pólvora foi bastante utilizada nos últimos séculos, principalmente, no século XX, durante a 1ª e 2ª Guerra Mundial. Geralmente, a descoberta da pólvora é atribuída aos chineses, que aparentemente a fizeram por volta do ano 1000 d.C. ou seja, por volta do século XI. Foi também os chineses que inventaram os fogos de artifício. Não como eles são encontrados hoje, mas de uma forma primária.
Na Europa, como é de conhecimento de muitos, ocorreram diversas guerras, dentro e patrocinadas por seus países. Isso ajudou no desenvolvimento de técnicas de trabalho com a pólvora e até a sua melhoria. Neste continente, a pólvora chegou por volta do século XIII ou XIV, mas só no século XVIII, durante a Revolução Francesa que a sua produção foi melhorada. Antoine Laurent Lavoisier, durante esta revolução, foi nomeado como o responsável pela munição, ou seja, pela pólvora, já que possuía conhecimentos em química. Até então, o salitre utilizado na produção de pólvora era obtido de forma primitiva e em pequenas quantidades. Lavoisier foi quem descobriu uma maneira de sintetizar o salitre em grandes quantidades, o que possibilitou um aumento sensível na produção e utilização da pólvora.
A pólvora, em um fogo de artifício, possui, além do nitrato de potássio (KNO3), perclorato de potássio (KClO4) ou clorato de potássio (KClO3). Estes compostos são denominados oxidantes e são altamente explosivos. A presença desses sais (KClO4 e KClO3) é uma forma de aumentar a explosão e a claridade proporcionada pelo fogo de artifício. Geralmente é utilizado sais de potássio, mas não de sódio, isso é devido ao fato dos sais de sódio absorverem água da atmosfera com maior facilidade do que os sais de potássio. Esse fato é o que impossibilita a utilização de sais de sódio em fogos de artifícios, uma vez que ao serem estocados, caso fossem feitos com sais de sódio, ocorreria a absorção de água, o que atrapalharia no momento da explosão do fogo. Além da intensa luz amarela que é obtida com os sais de sódio, que ofuscaria as outras cores.
A Química das cores dos fogos de artifício
As cores produzidas em um show de fogos de artifício são produzidas a partir de dois fenômenos, a incandescência e a luminescência.
Incandescência
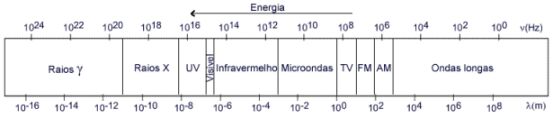
A incandescência é a luz produzida pelo aquecimento de substâncias. Quando se aquece um metal, por exemplo, ele passa a emitir radiação infravermelha, que vai se modificando até se tornar radiação visível na cor branca. Isso irá depender de qual temperatura é atingida. Um exemplo de incandescência são as lâmpadas incandescentes, onde existe um filamento de tungstênio que é aquecido e passa a produzir luz, a partir da incandescência. Este fenômeno é, também, visto nos fogos de artifício, nos quais são utilizados metais como o alumínio e magnésio, que ao queimarem produzem alta claridade.
Luminescência
A luminescência é a luz produzida a partir emissão de energia, na forma de luz, por um elétron excitado, que volta para o nível de energia menos energético de um átomo.
| Este fenômeno, a luminescência, pode ser explicado da seguinte forma: 1) Um átomo, de um elemento químico qualquer, possui elétrons em níveis de energia. Ao receber energia, estes elétrons são excitados, ou seja, são promovidos a níveis de energia mais elevados. A quantidade de energia absorvida por um elétron é quantizada, ou melhor, é sempre em quantidades precisas, não podendo ser acumulada. 2) O elétron excitado tem a tendência de voltar para o nível menos energético, pois é mais estável. Quando ocorre esta passagem, do nível mais energético para o menos, ocorre também a liberação da energia absorvida, só que agora, na forma de um fóton, ou seja, na forma de luz. |
A luminescência é uma característica de cada elemento químico. Ou seja, átomos de sódio quando aquecido, emitem luz amarela, pela luminescência. Já os átomos de estrôncio e lítio produzem luz vermelha. Os de bário produzem luz verde e assim por diante.
Os fogos de artifício utilizam deste fenômeno e desta variedade, uma vez que há fogos das mais diversas cores. No entanto, nos fogos de artifício são utilizados sais destes elementos químicos, pois o elemento puro, é muitas vezes, reativo. Na tabela a seguir, há uma relação entre as cores e os sais dos elementos químicos utilizados para a sua produção.
|
Sais de sódio, tais como: NaNO3, Na3AlF6 e NaCl
|
|
Sais de cobre, tais como: CuCl2 e Cu3As2O3Cu(C2H3O2)2
|
|
Sais de cálcio, tais como: CaCl2, CaSO4 e CaCO3
|
|
Sais de estrôncio e lítio, tais como: SrCO3 e Li2CO3
|
|
Sais de bário, tais como: Ba(NO3)2e BaCl+
|
|
Mistura de sais de estrôncio e cobre
|
|
Alumínio e magnésio, metálicos ou sais
|
|
Referência Bibliográfica
1-KOTZ, J., C., TREICHEL, P., Química e Reações Químicas, 3ª edição, volume 2; Rio de Janeiro, Editora LTC, 1998.
2-Tosi, L. Química Nova. 1989,12(1), 33-56.
|





 O gás carbônico é também um gás produzido a partir da queima/combustão completa de material orgânico (composto formado principalmente por átomos de carbono e hidrogênio, podendo conter heteroátomos), que ocorre na presença de
O gás carbônico é também um gás produzido a partir da queima/combustão completa de material orgânico (composto formado principalmente por átomos de carbono e hidrogênio, podendo conter heteroátomos), que ocorre na presença de  Nas águas naturais, tais como rios, lagos e oceanos há grande volume de dióxido de carbono dissolvido e na forma de carbonatos, como os presentes nas conchas de moluscos marinhos. Na forma de calcário, o CO2 pode ser encontrado em rochas calcárias, que nada mais são do que calcários metálicos, como o carbonato de cálcio (CaCO3) ou o carbonato de sódio (Na2CO3).
Nas águas naturais, tais como rios, lagos e oceanos há grande volume de dióxido de carbono dissolvido e na forma de carbonatos, como os presentes nas conchas de moluscos marinhos. Na forma de calcário, o CO2 pode ser encontrado em rochas calcárias, que nada mais são do que calcários metálicos, como o carbonato de cálcio (CaCO3) ou o carbonato de sódio (Na2CO3).
 O oxigênio é um elemento representativo e ametal, que se encontra no 16º grupo da
O oxigênio é um elemento representativo e ametal, que se encontra no 16º grupo da